



2月19日,CDE官网公示,中盛溯源(广州)生物科技有限公司申报的“NCR101注射液”获批临床默示许可,拟用于治疗间质性肺病(ILD)。据了解,NCR101是全球首款获批临床的诱导多能干细胞(iPSC)来源的基因修饰间充质样细胞(MSC)治疗产品,也是中盛溯源继“NCR100注射液”后第二款获批临床的iPSC来源MSC(iMSC)产品。
图片来源:CDE官网
“NCR101”——首款基因修饰iMSCplus
iPSC具备无限扩增的能力,可为现货型细胞治疗产品提供稳定且无限的种子细胞来源。“NCR101”作为iMSC产品,不仅能够实现规模化生产,还可以确保不同批次间iMSC的高度同质性,显著提高细胞治疗产品的一致性和可靠性。
更重要的是,“NCR101”利用iPSC易于基因工程化改造的特性,通过基因修饰技术进一步增强了iMSC疗效,可为ILD治疗提供更多可能性。
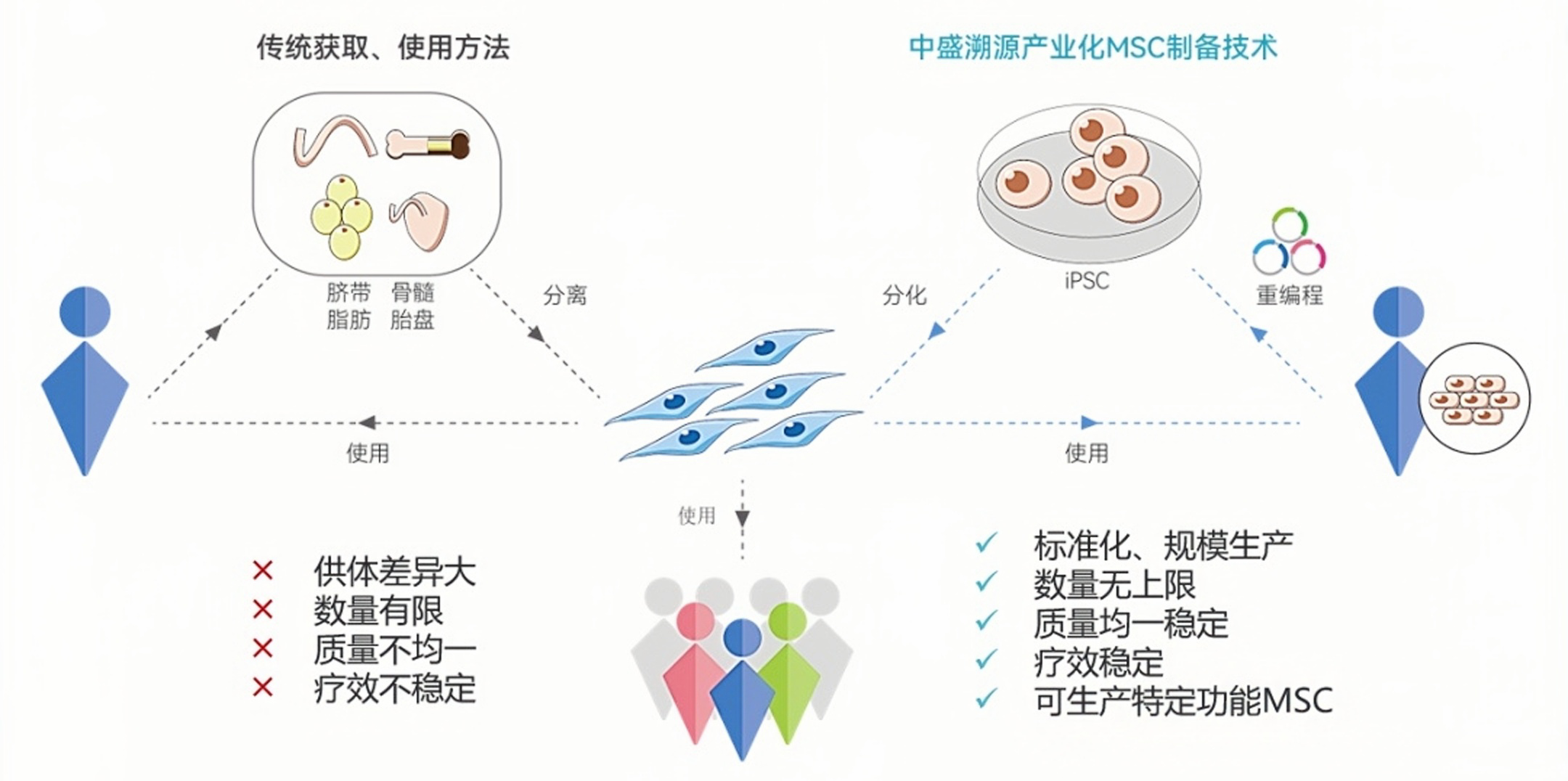
传统组织来源MSC vs. iMSC
值得注意的是,在ILD治疗领域,“NCR101”是首款获批临床的基因修饰MSC产品,也是首款获批的iMSC产品。
此前的临床研究可以发现,传统MSC多为组织来源,在规模化应用中存在诸多挑战。一方面,不同组织如脐带、骨髓、脂肪和牙髓来源的MSC,在表面标志物表达、免疫调节功能和增殖分化能力等方面表现出异质性;另一方面,这类MSC还面临一个根本性问题,即从单个组织分离获得的MSC数量与成人治疗所需的MSC数量相距甚远。
对于细胞疗法来说,最重要的就是在临床前端如何获得质量保证和数量充足的细胞药物,而iPSC技术相对来说就是比较理想的技术平台。相较于组织来源MSC,“NCR101”在产量、批间一致性和药效表达增强等方面具有显著的优势,展现出更优异的成药性。
从经济学角度来看,“NCR101”的生产工艺更易于标准化、规模化,能够大幅降低生产成本,契合中国医疗领域“降本增效”的政策方向。同时,其规模化生产能力可以更好地满足国内庞大的患者群体需求,降低治疗费用,减轻患者经济负担,具有显著的社会效益和经济优势。
此外,在治疗IPF(特发性肺纤维化)等罕见病领域,“NCR101”作为创新疗法,符合国家针对罕见病药物的政策支持,可享受优先审评、加速审批等政策支持,从而加快产品上市进程,尽早惠及患者。
关于中盛溯源
中盛溯源专注于开发广泛可及的iPSC衍生细胞治疗产品。未来,将继续在抗炎修复、肿瘤免疫和再生医学三大领域持续推进多类细胞药物管线的研发。目前,“NCR100注射液”(iPSC来源间充质样细胞,iMSC)治疗膝骨关节炎已推进至2期临床;“NCR300注射液”(iPSC来源自然杀伤细胞,iNK)治疗骨髓增生异常综合征、预防allo-HSCT后AML复发处于1/2期临床,后续针对其他适应症的iPSC来源细胞也将陆续进入注册临床试验阶段。